Не пахнут магазинские цветы? Обработайте их аммиаком. От его паров многие бутоны начинают благоухать. Хотя, запах самого аммиака довольно резок.
Вспоминаются нашатырь и пары мочи. Самыми чуткими к аммиаку цветами являются астры. Их аромат усиливается примерно в 6 раз.
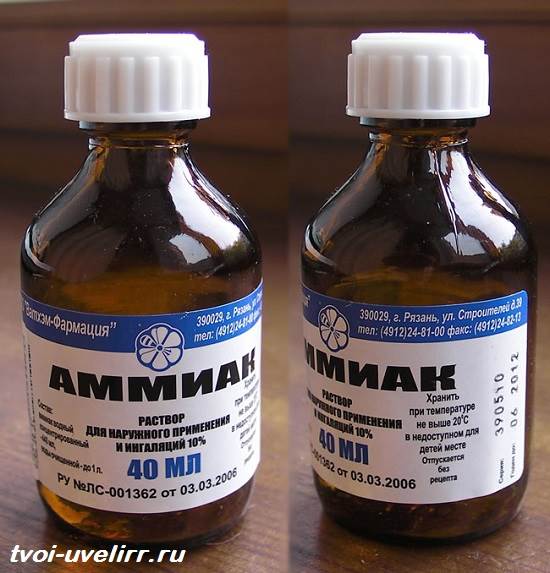
Изменить можно и цвет бутонов. Так, от паров реагента голубые и синие лепестки зеленеют, а красные – чернеют.
Флористам, как говориться, на заметку. Однако, аммиак пригождается и в других сферах деятельности. Узнаем остальные свойства вещества, ознакомимся с путями его применения.
Свойства аммиака
Работая с парами аммиака, стоит быть осторожным. При определенной концентрации смесь реагента с воздухом взрывоопасна.
К тому же, газ токсичен. «Общение» с ним чревато нервными расстройствами, ухудшением слуха, частичной потерей памяти, помутнением хрусталиков глаз. Эти симптомы наблюдаются у людей, работающих на аммиачных производствах.
Пары аммиака всегда устремляются вверх, поскольку газ легче воздуха. Газом вещество является в обычных условиях. Для транспортировки и продажи аммиак сжижают.
Для этого нужно повышенное давление. Получают безводный концентрат. Для него существует 6221-90 ГОСТ.
Сжиженный аммиак в сосудах, все же, имеет газообразную фазу. Под давлением оба состояния вещества находятся в равновесии.
При этом, температура должна быть ниже критической, как и давление. Если будет больше 132-ух градусов и 11-ти мегапаскалей, равновесие нарушится.
Коэффициент объемного сжатия вещества в разы меньше коэффициента его расширения.
Если сосуд заполнен доверху, повышение температуры может привести к давлению в 52 мегапаскаля.

Этого достаточно, чтобы разорвать металлические швы вмещающего сосуда. Соответственно, будет взрыв.
Из концентрата аммиака можно получить раствор аммиака любой насыщенности. Хотя, человечеству пригождается и безводная версия.
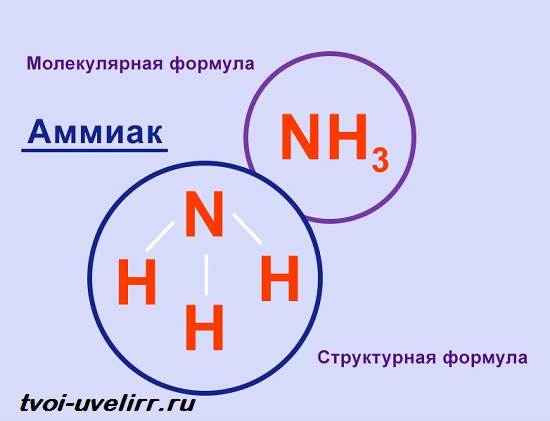
Она, к примеру, является одним из азотных удобрений. Кроме азота в веществе присутствует лишь водород. Последнего 3 атома, то есть, формула газа такова: — NH3.
Такое содержание водорода – причина отличной растворимости аммиака в воде. Другие газы этим «похвастаться» не могут.
Между аммиаком и водой образуются прочные водородные связи. Чем насыщеннее раствор, тем больше его растворяющие свойства.
По ним вещество конкурирует с этиловым спиртом, с той лишь разницей, что последний органического происхождения.
Так, аммиак водный, как и концентрат, способны растворить металлы щелочной и щелочноземельной групп.
Итогом реакций становятся темно-синие жидкости. Это результат ионизации валентных электронов и солватации.
Последнее понятие обозначает электростатический контакт между молекулами растворенных металлов и аммиака.
От нашатырного спирта запах аммиака исходит неспроста. Средство является водным раствором гидроксида аммония.
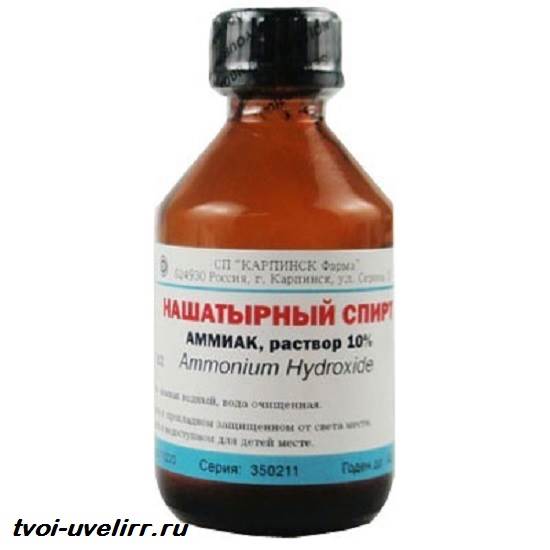
То есть, аммиак – это нашатырный спирт. Гидроксид аммония содержится и в моче, а так же, в продуктах разложения органики.
Именно поэтому, к примеру, неприятно пахнут гниющие массы со дна болот. В них разлагаются остатки растений, рыб, животных.
В тех же прудах аммиак, естественно, смешивается с водой. В растворе присутствует OH-группа.
Значит, смесь способна на щелочную реакцию, является слабым основанием. Растворяет героя статьи и спирт. Аммиак не случайно смешан с ним в нашатыре.
В концентрированном виде нитрид водорода сильно преломляет свет, то есть, меняет направление его лучей.
Еще одно любопытное свойство героя статьи – кипение при минусовых температурах. Должно быть около 34-ех ниже нуля.
Если опустить температуру до 78-ми градусов, жидкость, и вовсе, затвердеет. Получаются белесые хлопья, похожие на снег. Кристаллы вещества имеют правильную, симметричную форму.
Добыча аммиака
Производство аммиака сводится к 100 000 000 тонн ежегодно. Примерно столько же добывают хлора. При этом, аммиак менее токсичен.
В указанный объем аммиака входят вещество, извлеченное из природных источников азота, и синтезированное в искусственных условиях.
Промышленный метод основан на соединении водорода и азота. Аммиак из них получается при температуре не ниже 500-от градусов Цельсия.
Еще одно условие: — давление в 350 атмосфер. Не обойтись и без катализатора. Он ускоряет вялотекущую реакцию, сам в нее не вступая.
Роль катализатора, обычно, выполняет губчатое железо. Из более дорогих помощников выбирают оксид вольфрама, или платину.
Итоговый выход продукта при взаимодействии простых веществ равен примерно 30-35%.
Это максимум при соблюдении минимально возможной температуры и наибольшего давления. Именно такой дуэт обеспечивает эффективность реакции.
Однако, при нижней температурной планке уменьшается скорость процесса. Поддашь жару, — частично останешься без аммиака, зато, получишь его быстрее.
Синтетический метод производства аммиака практически не оставляет шансов его добыче в природе из продуктов гниения органики. Процесс этот долог.
Аммиак образуется, но быстро улетучивается. В ловушки земной коры газ попадает редко.
Обычно, аммиак понемногу испаряется, что делает природные месторождения неликвидными.
Применение аммиака
Применение вещества в сельскохозяйственной сфере уже упоминалось. Теперь, перейдем к индустрии красоты, вспомнив про аммиак для волос.
Здесь же вспомним, что раствор вещества является слабой щелочью. Отсюда назначение: — обеспечить щелочной Ph краски, в районе 10-ти.
Такая среда способствует набуханию волос, что запускает реакцию разложения перекиси водорода.
Последняя, является осветлителем, поэтому, обязательно используется в оттенках блонд.
Существует краска без аммиака. Однако, производители частично лукавят. Вместо чистого вещества применяются его производные.
Они тоже поднимают Ph до щелочного уровня, но стоят дороже. Соответственно, и краска для волос без аммиака требует затрат.

Однако, потребители готовы к ним, дабы сохранить здоровье шевелюры. Дело в том, что чистый аммиак сильнее раскрывает поры волос.
Они начинают напоминать губку, сгладить поверхность которой можно лишь дорогостоящей силиконовой косметикой, заполняющей пустоты.
Из продуктов питания выраженая щелочь – сода. На ее изготавление, так же, направлен синтез аммиака.
Производят его и для получения азотной кислоты. Аммиак преобразуют в оксид азота.
Последний, окисляют до диоксида. Потом, оксиды проходят абсорбцию водой. Так и получают кислоту.
Формула аммиака, как уже говорилось, лежит в основе создания взрывчатых субстанций.
Вещество нужно и на производстве холодильного оборудования. Его действие основано на испарении сжиженного газа. При этом, поглощается много тепла, что, собственно, и обеспечивает прохладу.
В ювелирном деле также не обошлось без аммиака. Его используют для очистки изделий из золота после полировки пастой ГОИ.
Потребности человечества в аммиаке отражает тенденция его производства. Еще 30 лет назад в год формировали 70 000 000 тонн реагента.
Теперь, как указывалось в главе «Добыча», — 100 000 000. Не поменялись лишь лидеры производства. Это, по-прежнему, США и, теперь уже, Россия.
В справочниках прошлых лет фигурирует, естественно, СССР. Что поменялась стоимость вещества, и гадать не надо. Ознакомимся с актуальным ценником на аммиак.
Цена аммиака
Аммиак купить можно оптом и в розницу. Крупные поставки осуществляют, как правило, тоннами.
За 1000 килограммов просят от 19000 рублей. Небольшие предприятия готовы продавать по килограмму, прося около 30-ти рублей.
В розницу килограммы предлагают редко, тонны не предлагают вовсе. Изучим прейскурант аптек, обратив внимание на нашатырный спирт.
Обычно, его разливают во флаконы по 40 миллилитров. Стоит такой объем от 15-ти до 31-го рубля.
Интересно, что, если встречаются флаконы на 25 и 100 миллилитров, стоят они примерно так же, от 13-ти до 55-ти рублей.
При этом, стоит учесть, что спиртовой раствор 10-процентный. Сжиженный же аммиак на оптовых поставках концентрированный.
Поэтому, промышленникам приходится задумываться о правильной транспортировке груза. Есть специальные полуприцепы с цистернами.
Возраст емкостей не должен превышать 30-ти лет. Важен и состав сплава для цистерн, ведь аммиак растворяет многие металлы.
Учитывать приходится, так же, давление в резервуаре, температуру. Поэтому, рядом с объявлениями о продаже реагента, как правило, размещают и предложения по продаже и аренде полуприцепов. Без них не обойтись.
